IV. Atome
Il n’y a pas d’accord sur l’illustration permettant de rendre compréhensible un atome.
Le modèle solaire est à oublier : les électrons ne peuvent tourner autour du noyau comme des planètes autour d’une étoile. Si c’était le cas, ils perdraient leur énergie par radiation puisqu’ils sont chargés électriquement et finiraient par tomber sur le noyau. Par ailleurs les trajectoires seraient perturbées par les chocs qui se produiraient entre les électrons. De plus ce modèle ne permet pas d’expliquer que les atomes aient le même comportement physique et chimique, d’où qu’ils viennent dans l’univers, avec exactement les mêmes trajectoires d’électrons autour du noyau.
L’électron n’est pas un point, mais une onde tant qu’on ne le mesure pas.
Plongée dans l’hydrogène
C’est le plus simple et le plus léger des atomes. Sa taille est de l’ordre d’un dixième de milliardième de mètres (10-10 m). Il est constitué d’un noyau comportant un seul proton et autour de lui d’un seul électron. Les deux charges électriques s’attirent. L’équation de Schrödinger permet de calculer l’effet de cette attraction. En lui fournissant le potentiel électrique créé par le noyau, on obtient la fonction d’onde, c’est-à-dire, pour faire simple, la forme de l’électron. Le noyau agit comme une sorte de cage électrique qui emprisonne l’électron, comme une sorte de filet électrique tendu autour de lui. Le noyau crée un piège électrique qui présente les mêmes effets qu’une boîte. La quantification opère donc ici aussi (cf. chap. III). La fonction d’onde de l’électron n’a plus droit qu’à certaines formes et certaines énergies spécifiques. La forme la plus simple d’entre elles, celle de plus basse énergie, ressemble à une boule pleine, un peu plus dense au centre qu’au bord.
Le noyau est constitué d’un simple proton, mesurant un millionième de milliardième de mètre (10-15 m), c’est-à-dire 100 000 fois plus petit que l’atome lui-même. Ce proton est régi par les règles de la quantique mais les forces et les masses qui le gouvernent sont gigantesques et relèvent de la physique nucléaire. Il est incroyablement dense et petit, presque ponctuel. Autour du noyau, se déploie l’électron, en comparaison très léger et volumineux. Il forme une sorte de nuage à l’allure sphérique de près d’un dixième de nanomètre (10-10 m) et presque 2000 fois plus léger que le proton. Ses bords ne sont pas nets : le nuage s’évanouit, progressivement.
Si on excite cet atome avec un rayon laser bien choisi, l’électron saute soudainement à une énergie plus élevée et sa fonction d’onde change brutalement pour adopter une nouvelle forme. Le nuage formé par l’électron devient plus gros. Cette sphère n’est pas simplement une trace du mouvement de l’électron autour du noyau. C’est plutôt la carte des possibles. Si on pouvait mesurer cet électron on le retrouverait quelque part dans cette sphère.
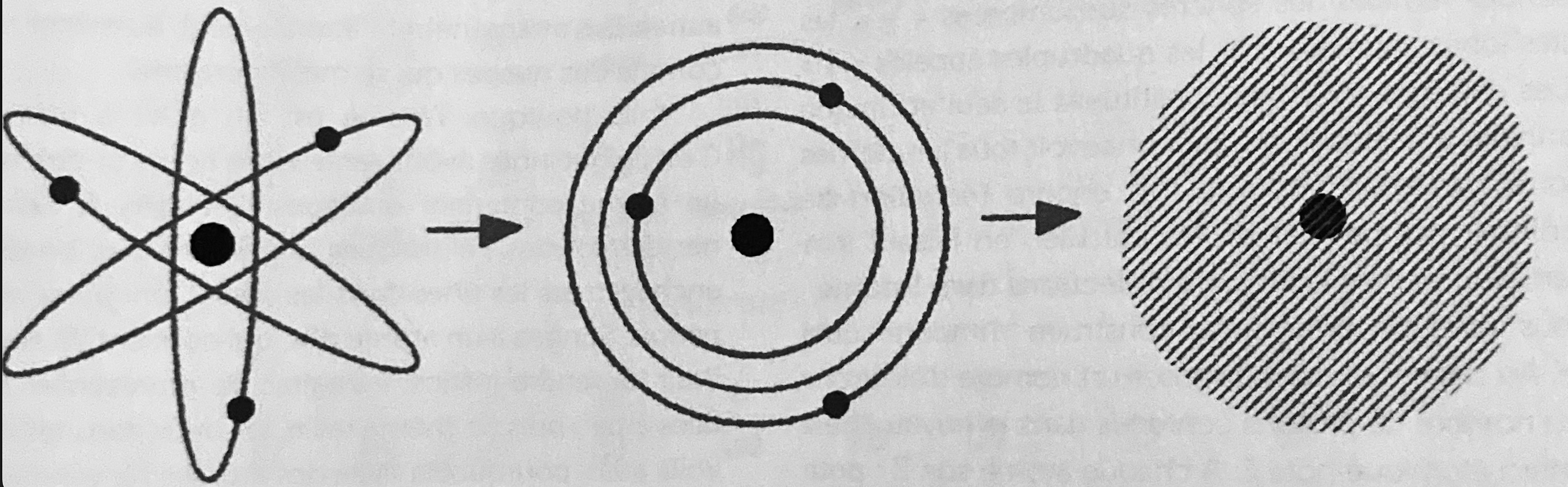
Au début de la quantique, le modèle planétaire (ici pour un atome d’hydrogène) a dû être abandonné au profit d’un modèle à orbites, le modèle de Bohr. Puis, celui-ci a laissé place à la vision actuelle de l’atome dans laquelle l’électron occupe tout un volume autour du noyau avec sa fonction d’onde quantique.
Un atome plus complexe : le carbone
Son noyau comporte six protons et six neutrons. Autour se trouvent six électrons. Pour déterminer la forme de chaque électron, il faut résoudre l’équation de Schrödinger. Les électrons sont négatifs et interagissent entre-eux et de ce fait le calcul devient bien plus compliqué, trop pour être résolu. On ne dispose toujours pas de solution exacte de l’équation de Schrödinger pour un atome de carbone ! Pour simplifier les physiciens supposent que chaque électron ne voit, en plus du noyau, qu’une espèce de gros nuage formé par les cinq autres électrons.
Toutes les formes possibles des électrons peuvent être calculées, de la plus basse énergie à la plus élevée, grâce à l’équation de Schrödinger. Étonnamment, on n’obtient pas que des sphères de plus en plus grosses. Les électrons adoptent des profils en forme de doubles sphères, de doubles lobes, de quadruples lobes, de lobes opposés.
Ces fonctions d’ondes archétypales sont appelées des orbitales. Elles sont regroupées en grandes familles : les sphères nommées « s », les double-lobes appelés « p », les quadruples-lobes appelés « d ». Ces volumes constituent le seul et unique dictionnaire permettant de concevoir tous les atomes.
Chaque atome possède un numéro atomique égal au nombre d’électrons et donc au nombre de protons de son noyau. Pour construire n’importe quel atome, il faut suivre une règle unique : piocher les fonctions d’onde de ses électrons dans le catalogue fourni par l’équation de Schrödinger, en partant de la plus basse énergie et en augmentant d’un cran tous les deux électrons pour respecter le principe d’exclusion de Pauli (deux électrons de spins différents peuvent avoir la même forme, mais pas plus). Les électrons ne s’empilent pas les uns à côté des autres ou les uns au-dessus des autres comme les couches d’un oignon. Les électrons se mettent les uns dans les autres. Ils s’interpénètrent au même endroit comme des nuages qui se mélangeraient. Voilà pourquoi l’atome est un enfer à représenter.
Voici finalement ce à quoi ressemble véritablement un atome, ici l’atome de carbone. Ses 6 électrons s’interpénètrent les uns les autres, avec différentes formes d’orbitales.

L’atome d’or comporte 79 électrons. Il faudrait représenter 79 orbitales à peu près de la même taille les unes dans les autres.
C’est la raison pour laquelle la taille des atomes ne varie pas beaucoup entre les plus légers et les plus lourds. Si les électrons s’empilaient simplement, un atome d’or devrait être au moins 10 fois plus gros qu’un atome de carbone. Pourtant, il n’est que deux fois plus gros : sa taille est celle de son plus gros électron.
Comme la construction d’un atome suit toujours les mêmes règles et utilise toujours les mêmes formes d’électrons elle aboutit toujours exactement aux mêmes résultats. Un atome de carbone, d’où qu’il viennent, aura toujours précisément les mêmes propriétés et la même forme. C’est l’« identité de la matière ».
Le catalogue limité de formes d’électrons autorise une variété d’atomes très importante qui est responsable de la richesse et de la diversité extraordinaire du monde. En fait, c’est le tout dernier des électrons de chaque atome qui lui confère l’essentiel de ses propriétés et le distingue des autres. Par exemple l’hélium est un gaz inerte incolore presque indétectable. L’atome suivant dans le tableau périodique est le lithium. Il a un noyau un peu plus massif et chargé et surtout un électron en plus. C’est cet électron supplémentaire qui rend le lithium solide, métallique et hyper réactif. La forme de l’orbitale du dernier électron influence aussi la façon qu’aura l’atome de s’accrocher à ses voisins pour former les molécules. C’est la diversité des orbitales et des façons de les accrocher entre elles, qui autorise la variété des matériaux : des liquides, des gaz, des solides, des métaux, des isolants, des objets durs, mous, des couleurs, du brillant, du transparent, du magnétique, etc.
Si on cherche à mesurer un électron pour vérifier la forme de son orbitale, il se réduit soudainement en un point.